林逸贤:经导管二尖瓣钳夹术MitraClip的全球临床应用历程

▲ 林逸贤教授精彩演讲
从发病机制来看,
MitraClip如何发挥作用
▲▲▲
从发病机制上来讲,二尖瓣瓣叶关闭不全或脱垂导致左室收缩时血液反流进入左房,进而引起左室前负荷增大,导致或加重心衰症状。同时,这样一来又会导致二尖瓣瓣环扩大加重反流程度,形成恶性循环。从病因上来看,二尖瓣反流(MR)可分为原发性和功能性两大类,前者欧美以退行性病变居多,我国过去以风湿性病变居多,近年来则有向欧美看齐的趋势。
针对二尖瓣反流的发病机制,其治疗策略可分为瓣环成形、缘对缘修复(edge to edge)、瓣叶切除、腱索成形和左室成形。经导管二尖瓣钳夹术MitraClip原理非常简单,股静脉途径入路,在超声的引导下经房间隔将MitraClip送到合适的位置,将关闭不全的瓣膜夹合起来。2013年和2019年美国FDA分别批准了MitraClip在高危退行性MR和功能性MR中的应用。目前,MitraClip已经成为了世界范围内有显著症状的高龄MR患者的标准治疗手段。

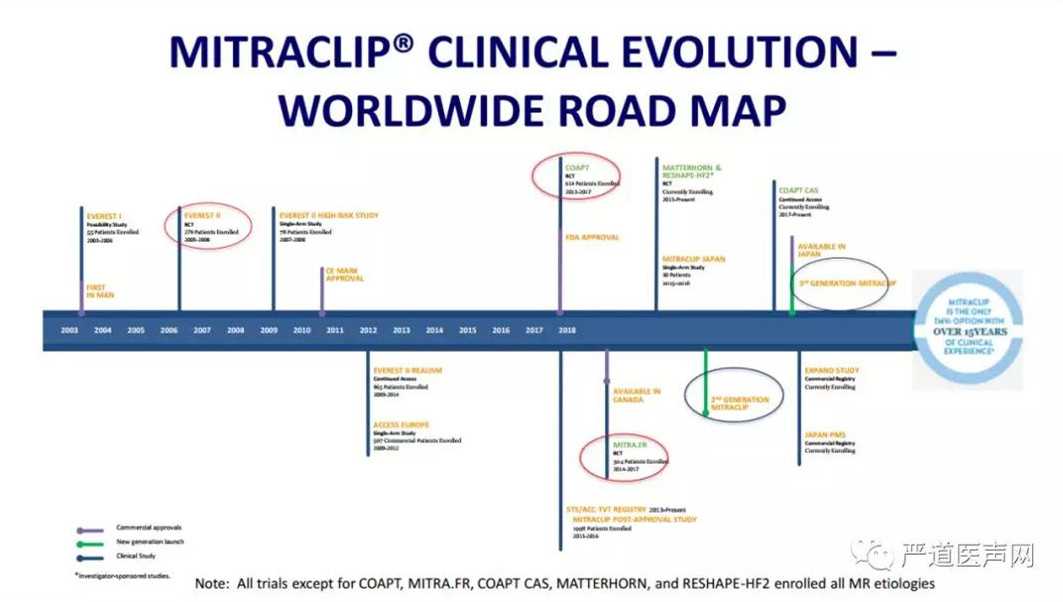
伴随着MitraClip漫长的临床研究历程, MitraClip在全球临床应用超过80,000例
EVERST II研究,
奠定MitraClip临床应用基础
▲▲▲
10余年前,EVEREST II研究横空出世,为MitraClip的临床应用奠定了基础。该研究为头对头研究,入选患者严格,以退行性或功能性、非风湿性A2/P2区域MR的患者为研究对象,其中大部分为二尖瓣脱垂患者,这类患者内外科治疗均可,旨在对比MitraClip与外科手术的效果。5年随访结果显示,两组患者死亡率并无显著差异,但MitraClip组再次外科手术率却显著高于外科治疗组。
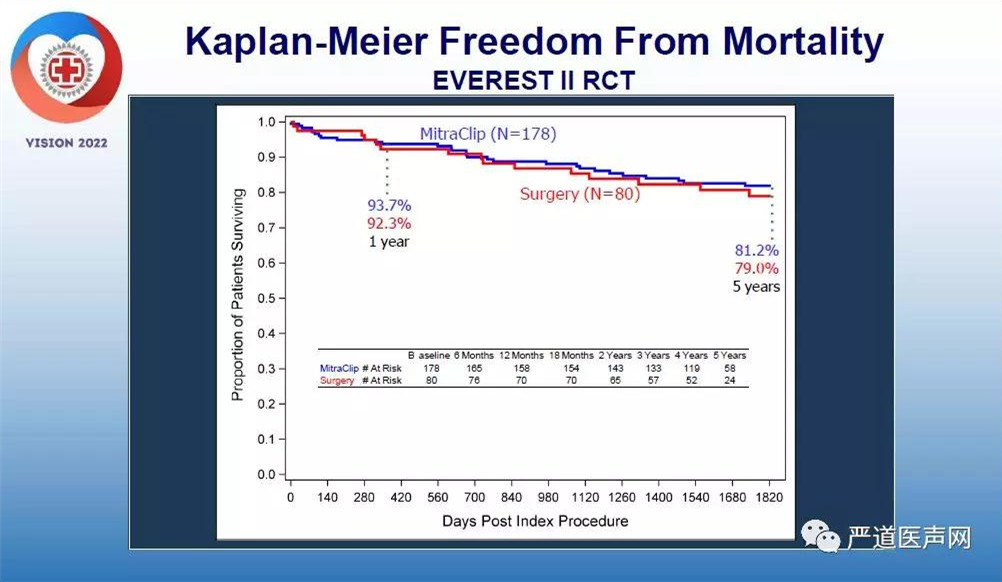
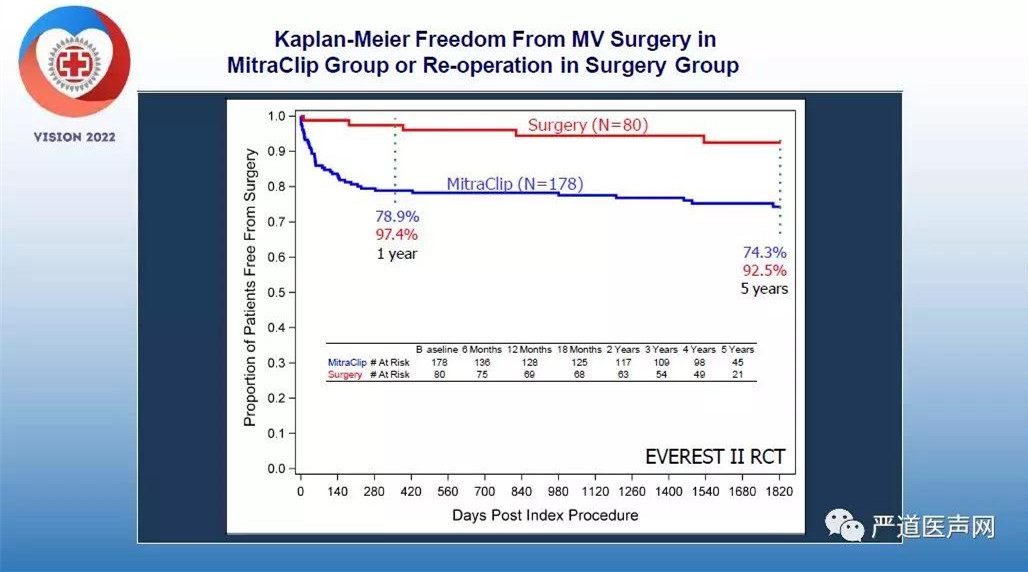
这样的结果是否能说明MitraClip效果不佳呢?其实不然,进一步分析发现,MitraClip组相当一部分患者再次手术发生于术后半年内,这说明,其实相当一部分选择MitraClip患者在首次手术时并没有达到很好的修复效果,这样一来直接导致了再次手术率的增加。而对于那些MitraClip手术效果满意的患者,其实再次手术率并非如此。
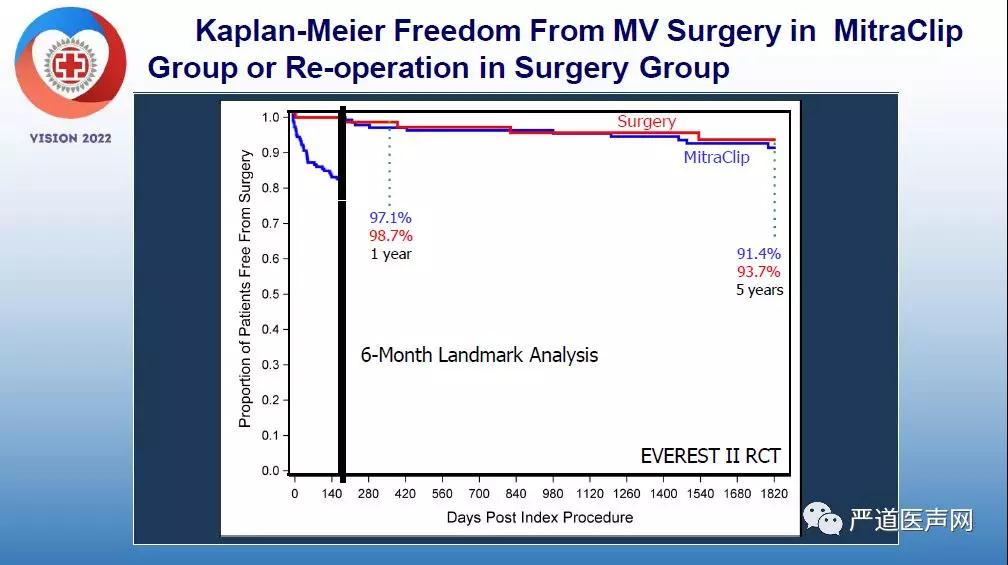
因此,我们认为,MitraClip仍是可以减少MR严重程度,改善左室功能和心功能,为MR患者带来与外科手术相当的临床获益。
GRASP研究,
MitraClip走上挑战复杂病变之路
▲▲▲
EVEREST II研究证实了MitraClip的临床效果,但其患者是具有高度选择性的。随着经验的积累,一些介入医师开始挑战MitraClip在更为高危或复杂的患者中的应用。GRASP研究根据患者是否满足EVEREST II研究的纳入标准,将其分为EVEREST ON组和EVEREST OFF组,评价MitraClip的临床效果。
分析患者特征我们可以发现,EVEREST OFF组病情较重,体现在LVEF值更低、左室更大、严重反流也更多。
MitraClip装置本身近年来也经历了几番革新,对于这种更为复杂的患者,我们可以植入多个夹子以达到最好的修复效果,使更多的患者免于开胸手术之苦。
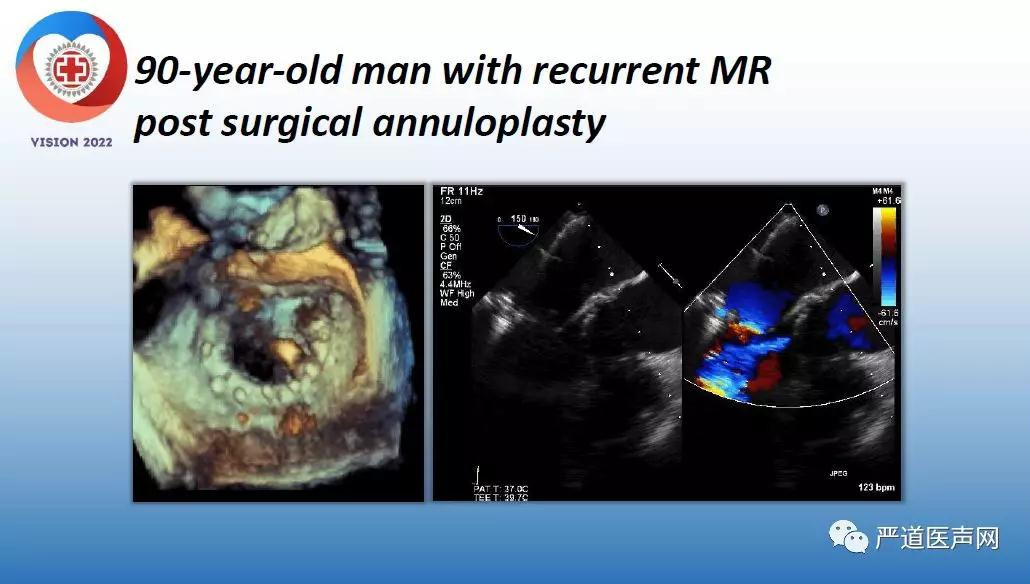
(90岁患者,外科治疗后仍残留严重二尖瓣反流,经MitraClip治疗后症状缓解)
COAPT研究,
MitraClip同样适用于功能性MR
▲▲▲
至于功能性MR,这类患者往往合并较多的心脏基础疾病,外科手术风险高,一项纳入9个研究的荟萃分析显示,对于需要搭桥手术的MR患者,在搭桥手术时同时行二尖瓣修复并未降低死亡率。指南在这方面也没有过多的给予积极的推荐。MitraClip的出现为这类患者带来了新希望。
提起MitraClip在功能性MR中的应用,就不得不提起设计相似、结果却迥异的Mitra-FR研究和COAPT研究。原因为何?仔细分析发现,Mitra-FR研究药物治疗组患者仅仅是基于医生经验调整用药,而COAPT研究则严格给予基于指南的药物治疗(GDMT),接受MitraClip治疗的患者均为药物治疗无效的高危患者。因此不难理解,COAPT研究为何会得出更为积极的研究结果。近期TCT 2019也公布了COAPT研究的3年随访结果。COAPT也不负所望为我们带来了期望的结果——无论是早期即接受MitraClip治疗还是药物治疗后心衰加重、挽救性植入MitraClip,均可带来获益。
最初,对于MR患者来说,外科手术是唯一治疗方法。经过近年来介入器械的不断发展,经导管介入治疗二尖瓣反流已经成为了中危患者的标准治疗手段,对于那些解剖结构不适合介入治疗的患者,我们考虑外科治疗。经导管二尖瓣修复器械领域也是百花齐放,MitraClip无疑是这百花丛中最受关注的那一支,其安全性及有效性已经得到充分证实,甚至可以将其称为外科手术4.0版本。
未来,在二尖瓣治疗领域,我们也需要介入医师、外科医师、影像医师更好地开展团队协作,才能更好地治疗患者。


